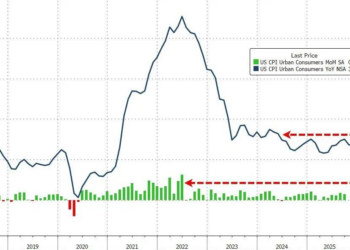
《科创板日报》1 月 8 日讯 (编辑 宋子乔) 北京时间 1 月 8 日凌晨,北大关于癌症疫苗的最新成果发表于 《自然》(Nature)——北京大学化学与分子工程学院陈鹏团队,联合席建忠团队以及深圳湾实验室团队,首次提出 「降解疫苗」新策略,为攻克癌症免疫耐受医学难题提供新路径。
降解型疫苗 iVAC 被用来撕掉肿瘤的 「隐身衣」、唤醒人体内沉睡的 「免疫大军」。
从细胞、小鼠到源自病人的类器官模型,在不同层面的实验中,iVAC 分子的功效被一次次验证。「看到所有小鼠的肿瘤生长都被有效抑制的那一刻,我很兴奋。相较传统的免疫检查点阻断疗法,iVAC 展现出了明显更好的抗肿瘤效果。」 第一作者之一、博士后韩雨表示。
《自然》 审稿人对此也给出了高度评价:「这是令人鼓舞的发现,为新型治疗手段的研发提供了重要的理论基石。」

陈鹏实验室合影
唤醒体内免疫系统的关键:解决癌症疫苗的 「瞄准」 痛点
癌症疫苗是一个极具前景但多数仍处于临床阶段的领域,核心思路是利用疫苗激活患者自身的免疫系统来攻击癌细胞。该疗法以人类自身免疫系统作为武器,被誉为继手术、放化疗之后的第三次抗癌革命。它不像传统疗法那样 「杀敌一千自损八百」,而是让患者身体里的免疫系统全力出击,消灭恶性肿瘤。
传统的癌症疫苗治疗思路,是让免疫系统通过识别身份标签来识别敌人。但这面临一个 「瞄准困境」:一般来说,肿瘤的 「身份标签」 取自肿瘤本身, 但很多肿瘤细胞表面缺少能被免疫 T 细胞识别的、独特的 「身份标签」(即肿瘤特异性抗原),同时,它们还主动穿上 「防护服」(如高表达 PD-L1 蛋白),成为所谓的 「冷肿瘤」。结果就是,对于 「冷肿瘤」,免疫系统即使大军压境,也像得了 「脸盲症」,看不见敌人,或者看见了也被强行抑制,导致治疗无效。
北大团队要解决的痛点,便是这一棘手的问题——如何让免疫系统 「看见」 并有效攻击那些擅长 「隐身」 的肿瘤。
其研究的创新点在于思维转换——不找 「身份标签」,直接插入 「攻击旗帜」。研究人员利用化学工具,一种叫 「瘤内疫苗嵌合体」(Intratumoural vaccination chimera,iVAC) 的新型分子,强行给肿瘤打上一个醒目的、免疫系统必然认识的标记,免疫系统从此不用费力辨认肿瘤细胞的身份标签。
研究人员将这一过程比喻为一场细胞层面的 「特洛伊木马」 行动:
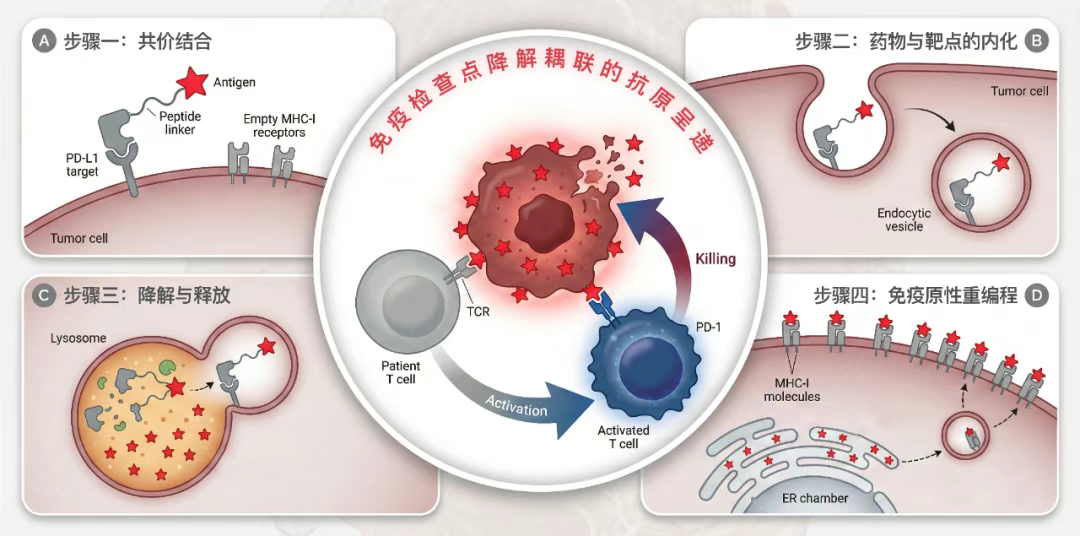
他们将 iVAC 小型嵌合分子视作 「特洛伊木马」,iVAC 分子先通过共价型纳米抗体的 「导弹头」 结合到肿瘤细胞表面;随后,在内化模块的驱动下,iVAC 和靶点蛋白被共同拉入细胞内,并进入具有降解能力的溶酶体中。
在此处,「敌方防御工事」PD-L1 蛋白被破坏,癌细胞的免疫刹车被松开,而研究者精心挑选的抗原肽段则被进一步加工,最终以多肽碎片组装复合物 (peptide-MH Ccomplex) 的方式出现在细胞表面,成为插在癌细胞头上的 「攻击旗帜」 的一部分,进而唤醒人体内沉睡的免疫军团。
尽管功能强大,这个 「特洛伊木马」 的身材却非常小巧 (分子量仅 18kDa)。这意味着它能在致密的实体瘤中穿梭渗透。
由此,一场细胞层面的 「特洛伊木马」 行动大获全胜。iVAC 分子将那些原本沉默的癌细胞,「重编程」 为高声呼救的免疫信使,高效激活了效应 T 细胞,其效果甚至与人体天然的免疫信使 (树突状细胞) 相当。这促成了免疫响应的正反馈循环,有效防止肿瘤复发。
目前,研究团队正在积极推进临床转化。得益于药物分子的模块化设计,未来团队可以针对不同患者,较快迭代出个性化的癌症疫苗,为癌症患者带来新的治疗希望。
放眼全球,癌症疫苗领域正处在一个从实验室向市场突破的关键节点,研发重点正从 「通用型」 疫苗转向 「个体化定制」,并探索与免疫检查点抑制剂 (如 PD-1 药物)、细胞疗法等联用,以克服肿瘤免疫抑制微环境,但成本和制备流程是其普及的主要障碍。