文 | 氨基观察
当 「小核酸」 和 「减肥药」 这两个资本市场的热门概念碰撞,想象空间被迅速放大。
2025 年 12 月 8 日,Wave Life Sciences 公布其 siRNA 药物 WVE-007 用于减重的 1 期临床试验结果,尽管数据仍处于早期,但这是全球首次披露 siRNA 在人群中取得减重相关临床数据的案例,且潜力可期。当日,Wave 股价暴涨 147.3%。
不到一个月后,1 月 6 日,Arrowhead Pharmaceuticals 披露了两款 siRNA 肥胖候选药物的临床数据,在合并 2 型糖尿病的肥胖患者中,ARO-INHBE、ARO-ALK7 均实现了内脏脂肪、总脂肪等身体指标的改善。消息发布后,Arrowhead 股价上涨 10.9%。
这种热情来得快退得也很快,Arrowhead 股价高开后随即回落,背后原因指向公司在公开披露中,刻意回避了 「体重下降」 这一减重领域的关键终点。
而事实上,在临床前动物研究阶段,这几款 siRNA「减脂明显、但体重下降有限」 的特征就已经可以观察到。
在 GLP-1 类药物已经被真实世界数据反复验证,并持续刷新减重天花板的背景下,现阶段小核酸药物 「只减脂、不减重」 的临床结果,显然难以令资本市场真正买账。
但有一点毋庸置疑,减肥药的创新浪潮会持续很久,小核酸药物正成为一大新变数。
/ 01 / 靶肝成了优势
与 GLP-1 主要通过中枢和胃肠道机制抑制食欲不同,小核酸药物与减重的衔接依赖于其在肝脏靶向递送方面的天然优势。
首先小核酸在设计上通过 GalNAc 递送系统靶向肝脏这个代谢器官,长期、稳定的基因敲降实现了季度级甚至更低频率的给药。
从机制上看,在肝脏–脂肪轴中,肝细胞在能量过剩状态下 INHBE 表达上调并分泌 ActivinE,影响脂肪细胞表面的 ALK7 受体并激活 SMAD2/3 信号,抑制脂解、线粒体氧化及白脂肪棕色化,降低能量消耗并促进脂肪储存。
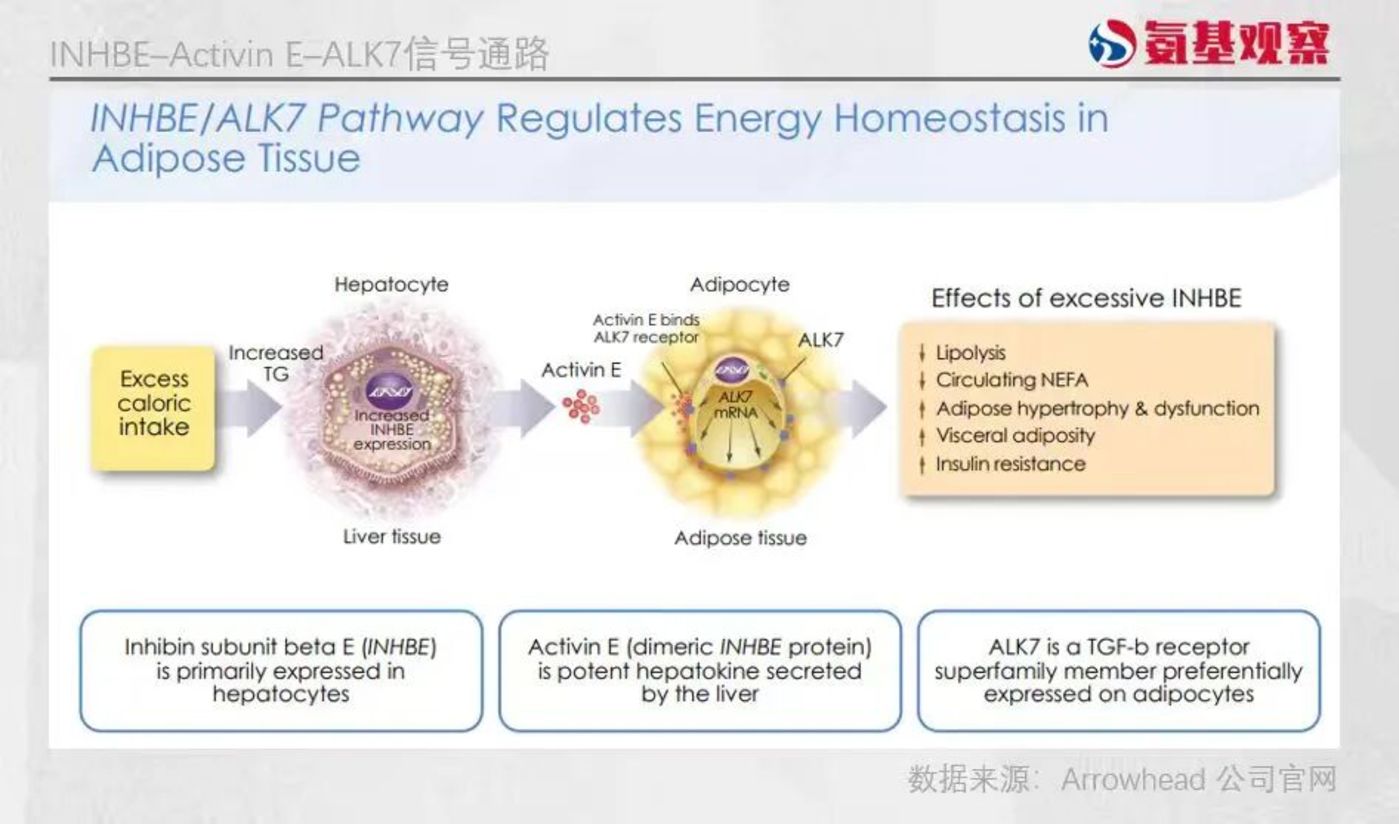
其中 INHBE 其表达水平与人类体重指数和胰岛素抵抗程度呈正相关。临床统计显示 INHBE 基因缺失与肥胖、2 型糖尿病之间存在直接关联。
因此,通过肝靶向 siRNA 下调 INHBE 表达,可从源头削弱 ActivinE 的内分泌输出,进而解除脂肪组织 ALK7 介导的代谢抑制,实现减脂效果。
目前全球围绕 INHBE 和 ALK7 的小核酸减重管线已经初具规模,其中 INHBE 靶点竞争格外激烈。2022 年 7 月 Alnylam 公司率先引入 INHBE siRNA 药物开发,后续被 Arrowhead 和 WAVE 赶超,后两者药物 Aro-INHBE、WVE-007 目前已公布临床 1 期数据。国内方面,大睿生物、圣因生物的同靶点产品已推进至临床阶段。
相比之下,ALK7 竞争局面要缓和很多。这主要是因为,ALK7 靶点与 TGF-β和活化素受体激酶高度相似,技术壁垒更高。海外目前仅 Arrowhead 产品 ARO-ALK7 进入临床阶段,ARO-ALK7 也被认为是全球首款明确靶向脂肪组织通路的 RNAi 疗法;国内同靶点包括圣因生物、苏州时安、舶望制药在内的多家公司相关项目仍处于临床前阶段。
早期动物试验的趋势验证了 siRNA 的减脂潜力:9mpk QW 的 ARO-INHBE 在小鼠中实现约 94% 幅度的 mRNA 敲低,达到 26% 减脂;同靶点 WVE-007 敲降效率 75%,总体重降低 10%。
但随着人体临床试验的结果公布,一些不容忽视的问题浮出了水面。
/ 02 / 减脂不减重
无论是 INHBE 还是 ALK7,目前 Arrowhead、Wave Life Sciences 披露的人体数据都出现了一致的矛盾:减脂水平与减重效果脱钩。
以 Arrowhead 为例,其新闻稿中几乎没有提供 ARO-INHBE 单药治疗患者的体重减轻数据,而是反复强调 「瘦体重保留」 这一指标。
此外,用药 12 周后,靶点敲降后反弹的现象已经出现,在低剂量组中尤为明显,这意味着持续性和稳定性仍有待验证。
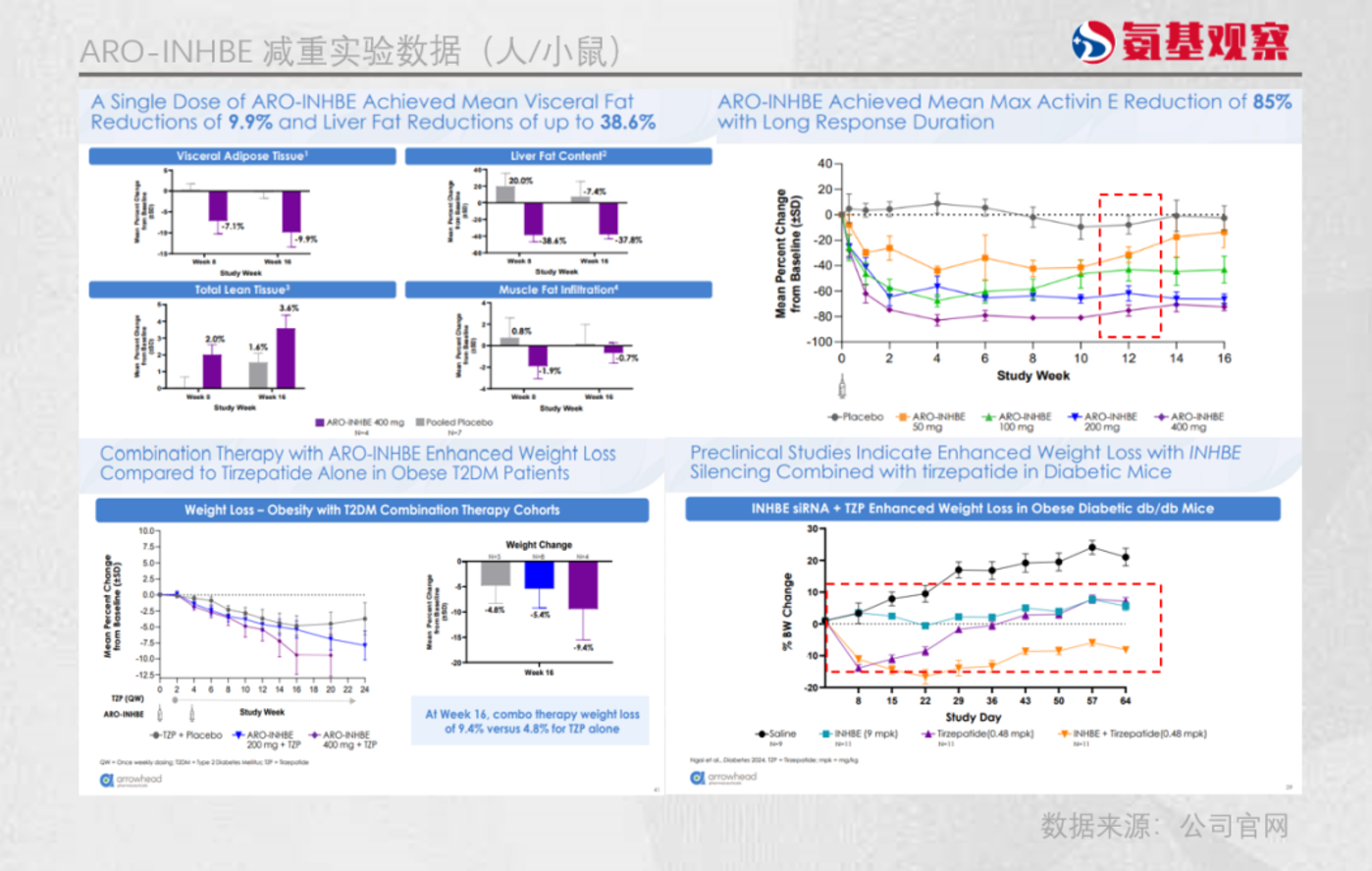
回到动物实验阶段,这些问题也并非毫无预兆。在相同模型下,小核酸靶点的减重效果明显弱于替尔泊肽 GLP-1/GIP 双靶点药物。
而从当前疗效看,ALK7 这一被认为 「更接近脂肪本身」 的靶点,目前也只能证明其在降低内脏脂肪方面优于 INHBE。ARO-ALK7 在 8 周内实现了约 13.6% 的内脏脂肪降低 (ARO-INHBE 为 9.9%),但同样缺乏同步披露的总体重变化指标。
WVE-007 的临床披露方式,则更取巧。240mg 三个月可以降低总脂肪 4.5%、降低内脏脂肪 9.4%、增加肌肉 3.2%,但其只公布了 240 mg 剂量组相较安慰剂额外降低 0.9% 体重的数据,市场猜测 WVE-007 在减重上并不明显。对此,公司的解释是,总脂肪的减少被瘦体重的增加部分抵消,导致总体重变化并不显著。
庆幸的是,上述药物在安全性上没有问题,绝大多数不良反应为轻中度。
但目前所有临床结果都是早期,样本量小且患者选择有 「代表性」,如女性占比高 (>60%) 等。因此仅披露均值、缺乏个体分布信息,使得患者异质性被大幅放大,进一步加剧了不确定性。
在这一背景下,小核酸若直接对标 GLP-1 类药物,无论从减重幅度还是临床竞争力来看,都缺乏优势。更严峻的是,当前监管机构对减重药物的审批核心标准,仍围绕体重下降指标展开。
这意味着,「只减脂、不减重」 的小核酸,在目前的监管框架下,难以获得认可。
/ 03 / 还要再等等
如今的减重市场正在从 「单纯体重下降」,逐步向 「减脂增肌、改善代谢指标」 转变。
从药物的机制来看,siRNA 也具有这方面的优势,但临床表现还未有定论。尤其是与 ActRII、GDF8 等已经证明可以同时实现减脂和增肌的靶点相比,小核酸效果显然不达标。
因此,小核酸药物在减重领域真正的机会或许在联合治疗。这也是在 GLP-1 占据大部分减重市场后,药企在该领域达成的共识。典型如 FGF21、Amylin 等在单药阶段已经展现一定减重潜力的靶点,但诺和诺德、礼来最终仍选择将其纳入联用体系,而非单独推进。
与此同时,小核酸的靶点也值得继续挖掘。比如 Canary Cure 的 CCT-217,尝试通过 ZNF423/CB1 双靶点,同时抑制脂肪细胞分化与食欲调控;又比如以 miR-22 为代表的非编码 RNA 方向,仍处于早期验证阶段,但为小核酸减重提供了更多可能性。
总之,这是一场充满机遇与未知的研发竞赛。药企对小核酸的追逐也在继续,1 月 13 日,中国生物制药公告称,将以总价 12 亿元,收购国内 siRNA 创新药企赫吉亚,后者管线包含 INHBE siRNA HJY-10。
在减肥领域,小核酸药物的发展才刚刚起步,远未到 「颠覆」 的阶段。
在 GLP-1 已经占据主导地位的现实下,小核酸更合理的定位,或许是作为长期、低频给药的代谢调节,以及长期体重维持管理。当然,一切还需要探索者们用临床数据来证明自己。