文 | 医曜
本文系基于公开资料撰写,仅作为信息交流之用,不构成任何投资建议。
12 月 1 日,美国 Biotech 公司 Janux 更新了 PSMA/CD3 屏蔽肽双抗 JANX007 的临床数据。不同于去年 12 月小范围试验的技惊四座,JANX007 的 1a 期期数据严重不及预期:PSA50(前列腺特异性抗原下降 50%) 由 100% 下降至 73%,PSA90 由 63% 骤降至 26%,ORR 由 50% 降至 30%。
不及预期的临床数据导致 Janux 公司股价盘后暴跌 44%,几乎一夜回到解放前。Janux 失败背后,则是前列腺癌所存在的巨大临床需求。
在男性恶性肿瘤的“ 死亡榜单” 上,前列腺癌仅次于肺癌,是全球男性第二大高发癌症 (全球每年约有 146.8 万新发病例,导致 39.7 万人死亡),而且还是中国增速最快的男性恶性肿瘤,近十年发病率年均增速高达 12.1%,已超越膀胱癌位居泌尿系统肿瘤首位。
从 1941 年休斯敦医生发现“ 去势手术可缓解前列腺癌进展” 开始,人类与这种疾病的对抗已持续八十余年。由最初的手术去势到如今的精准靶向,治疗理念不断迭代,可耐药、转移、副作用等问题始终难以突破。直到近几年,PARP 抑制剂、核素治疗、新型免疫疗法等创新手段的出现,前列腺癌治疗迎来了新的曙光。
一场持久战
前列腺癌 (prostate cancer,PCa) 是发生在男性前列腺的上皮性恶性肿瘤,50 岁前极少发病,50 岁以后随年龄增加发病率逐渐升高。目前前列腺癌发病率位于全球男性恶性肿瘤第二位,仅次于肺癌;在欧美发达国家尤为显著,是当地男性健康的头号威胁。
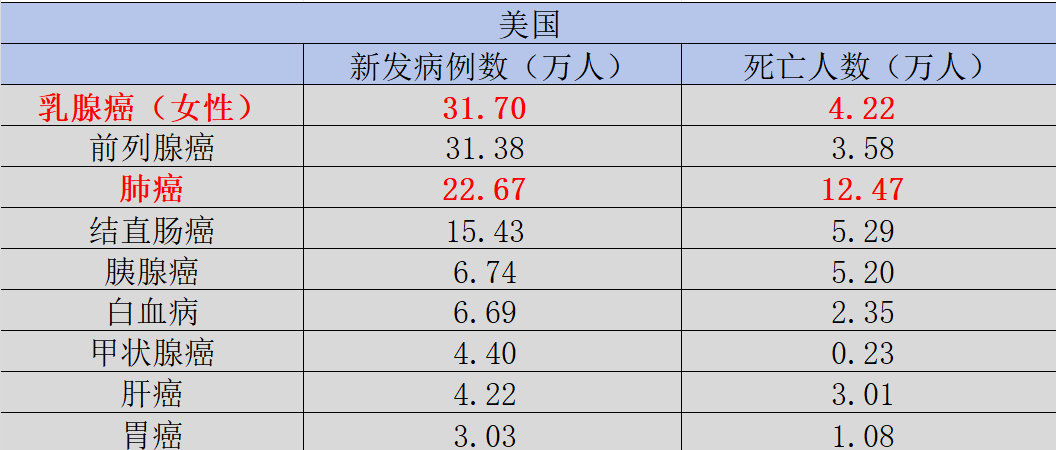
图:美国癌症发病与死亡,来源:锦缎研究院
可是前列腺癌的发病机制尚未完全明确,目前认为是遗传、激素、环境和生活方式等多种因素相互作用的结果。约 10% 的患者表现出家族聚集性,已确认的易感基因包括 DNA 损伤修复基因 (如 BRCA1/2、ATM)、错配修复基因及 HOXB13 等。此外,年龄增长导致的激素微环境改变,以及饮食、微量元素、肥胖、性激素、吸烟、环境等因素也被认为是前列腺癌发生的可能及潜在危险因素。
聚焦分子微观层面,雄激素受体 (AR) 信号通路的异常激活被认为是推动疾病发生发展的主要因素。雄激素通过与雄激素受体结合,调控下游靶基因的转录,影响前列腺细胞的增殖、分化和凋亡。这一通路的持续活化,特别是在去势抵抗阶段,与 AR 基因扩增、点突变、剪接变异体的产生以及共调节因子表达改变等多种机制相关。
1941 年,Huggins 开创性地发现手术去势 (睾丸切除术) 可延缓前列腺癌进展,揭示了该疾病与雄激素的密切关联。Huggins 也凭借这一发现于 1966 年荣获诺贝尔奖,其开创的雄激素剥夺治疗 (ADT) 原理,至今仍在临床实践中发挥着基石作用。
然而,手术创伤与心理影响让患者极难接受手术去势。直至 1980 年代促性腺激素释放激素激动剂 (如戈舍瑞林) 问世,以药物去势替代手术去势,成为转移性前列腺癌初始治疗金标准。

1990 年代,一代 AR 抑制剂比卡鲁胺上市,通过阻断 AR 与雄激素结合增强疗效,形成“ADT+一代 AR 抑制剂” 经典方案。2010 年后二代 AR 抑制剂实现质的突破:恩扎卢胺多环节阻断 AR 信号,阿比特龙通过抑制 CYP17 酶阻断肾上腺源性雄激素合成,两者将去势抵抗性前列腺癌 (CRPC) 患者中位生存期从 1 年延长至 3 年以上,迅速占据主要市场。
数据显示,2023 年全球前列腺癌市场规模约 129.8 亿美元,预计 2032 年将达 275 亿美元,其中中国市场预计将超过 200 亿元 AR 靶向药物占比超 60%,成为市场绝对主力。
但是,AR 治疗的光环下隐藏着难以逾越的困境。随着治疗时间延长,几乎所有的患者最终都会出现耐药现象,疾病进展为更具侵袭性的去势抵抗性前列腺癌。AR 基因扩增、点突变 (如 T878A)、剪接变异体 (如 AR-V7) 产生等机制,会使药物对 AR 信号的阻断失效。
长期 AR 信号阻断带来的生活质量影响同样不容忽视。疲乏、潮热、认知功能障碍、骨质疏松及代谢异常等系列副作用,不仅严重影响患者的日常生活质量,还可能导致患者因无法耐受副作用而中断治疗。
因此,无论是饱受耐药进展与副作用折磨的患者,还是深陷治疗瓶颈、亟待突破的市场,都对开发全新作用机制的药物,有着前所未有的迫切渴求。
“ 药王” 折戟
Janux 的失败并不丢人,因为这个赛道早已“ 哀鸿遍野”。
当前列腺癌的 AR 靶向治疗陷入瓶颈,医学界自然将目光投向了在多个癌种中取得突破的免疫疗法。
早在 2010 年,全球第一款癌症治疗疫苗 sipuleucel-T 就获批用于治疗前列腺癌。作为一款自体树突状细胞疫苗,sipuleucel-T 通过激活患者自身免疫系统识别肿瘤抗原,但 III 期临床试验显示其虽能轻微延长无症状或轻微症状的 mCRPC 患者总生存期,却未带来显著的肿瘤缩小,客观缓解率不足 5%,临床价值有限。
随后,CTLA-4 抑制剂 Ipilimumab 作为首个上市的免疫检查点抑制剂,单药用于 CRPC 患者时,因毒性反应显著且未达到预设的生存期终点宣告失败,联合治疗探索也未能突破疗效瓶颈。
这两款药物的折戟,并未浇灭行业对免疫治疗的期待,而是将目光聚焦于彼时已在多个实体瘤中大放异彩的 PD-1 抑制剂。其中“ 药王” 帕博利珠单抗 (K 药) 作为全球首个获批横跨黑色素瘤、肺癌、胃癌等数十个适应症的免疫检查点抑制剂,累计销售额已超千亿美元。其在黑色素瘤、非小细胞肺癌等领域创造的“ 长期生存” 奇迹,让行业普遍认为,这款广谱抗癌利器也能够打破前列腺癌的治疗困境。
可现实却给了科研界和市场沉重一击,K 药在前列腺癌领域的重磅临床研究先后遭遇失败。2019 年公布的 KEYNOTE-199 试验,是 K 药单药治疗 mCRPC 的 II 期临床研究,结果显示:PD-L1 阳性组 ORR 仅 5%,阴性组仅 3%,与传统化疗相比无显著优势,未达到预设终点。
此后,默沙东又启动了 4 项 III 期试验,但却以全军覆没告终。KEYLYNK-010 是 K 药联合 PARP 抑制剂 (奥拉帕利),因未能达到 OS 和 rPFS 双重主要终点,并且还与 3-5 级不良事件发生率的提高相关,最终宣布终止研究;KEYNOTE-921 是 K 药联合化疗 (多西他赛),试验 OS 和 rPFS 无统计学显著改善,仅呈趋势性提升;KEYNOTE-991 和 KEYNOTE-641 是 K 药联合恩扎鲁胺和 ADT,治疗转移性激素敏感性前列腺癌和转移性去势抵抗性前列腺癌,也因未达到改善 OS 和 rPFS 的主要终点而终止。
不止 K 药,纳武利尤单抗、阿替利珠单抗等其他 PD-1/PD-L1 抑制剂的相关 III 期试验也均未取得阳性结果,仅在微卫星不稳定 (MSI-H)、错配修复缺陷 (dMMR) 等极少数特殊亚型中显示出有限活性。
免疫抑制剂在前列腺癌领域的集体受挫,根源在于前列腺癌是一种典型的“ 冷肿瘤”,免疫微环境与免疫原性的先天缺陷让其难以对免疫检查点抑制剂产生应答。其肿瘤突变负荷极低,新抗原产生稀少,无法有效激活 T 细胞精准识别肿瘤;免疫微环境抑制则表现为肿瘤相关巨噬细胞以免疫抑制型 M2 为主,调节性 T 细胞增多,共同压制抗肿瘤免疫反应。
更独特的是,最新研究发现前列腺癌细胞自身能够表达并分泌 PD-1 分子,这些癌细胞来源的 PD-1 可通过外泌体途径激活骨髓细胞中的 JAK-STAT3 通路,进一步促进 MDSC 的扩增,从而加剧免疫抑制。
K 药的失败,并非免疫治疗在前列腺癌领域的终点,这场失败也为后续研发指明了方向,必须通过联合治疗手段重塑肿瘤微环境,将 “ 冷肿瘤” 转化为 “ 热肿瘤”,才能让免疫治疗发挥作用。也为 PARP 抑制剂、核素治疗等创新疗法与免疫治疗的联合应用埋下了伏笔。
创新时代
当传统 AR 靶向治疗遭遇耐药瓶颈,免疫单药治疗又在“ 冷肿瘤” 面前屡屡受挫时,医学界开始将希望寄托于更具创新性的治疗策略。
阿斯利康与默沙东联合开发的 PARP 抑制剂奥拉帕利,开创了前列腺癌精准治疗的新时代。前列腺癌中 20%-30% 存在 BRCA1/2、ATM 等 DNA 损伤修复基因 (HRR) 突变,这类细胞依赖 PARP 酶修复 DNA。奥拉帕利通过抑制 PARP 活性阻断修复通路,使肿瘤细胞因基因组不稳定凋亡,同时对正常细胞损伤极小。III 期 PROfound 试验证实,在二代 AR 抑制剂耐药的 HRR 突变 mCRPC 患者中,奥拉帕利中位 OS 达 19.1 个月,较传统方案延长 4.4 个月,ORR 达 33.3%,是对照组的 14 倍。
诺华研发的核偶联药物 Pluvicto(177Lu-PSMA-617) 通过精准靶向前列腺特异性膜抗原 (PSMA),实现了对肿瘤细胞的精准打击。PSMA 在 90% 以上 mCRPC 细胞表面高表达,为靶向递送提供了理想靶点。该药物由靶向 PSMA 的小分子配体和放射性同位素 Lu-177 组成,能够选择性地将辐射剂量递送至 PSMA 阳性的肿瘤细胞及其微环境,同时最大限度地减少对正常组织的损伤。临床研究显示,与更换 ARPI 方案相比,Pluvicto 将患者的中位影像学无进展生存期 (rPFS) 从 5.6 个月延长至 11.6 个月,疾病进展或死亡风险降低 59%(HR=0.41)。
与此同时,更前沿的技术如 PROTAC 和 ADC 等新兴疗法正从实验室快速走向临床。
与传统抑制剂不同,PROTAC 通过“ 降解” 而非“ 抑制” 靶蛋白,可更彻底地阻断信号通路,且不易因靶蛋白突变产生耐药。BMS 的 BMS-986365 是全球首款进入 III 期阶段的靶向 AR 的 PROTAC 药物,与 AR 拮抗剂恩扎卢胺相比,BMS-986365 在抑制 AR 驱动的基因转录方面的效力高出约 100 倍,在抑制各种前列腺癌细胞系中的 AR 依赖性增殖方面的效力高出 10 至 120 倍。
ADC 作为精准肿瘤治疗的重要平台,近年来在多种实体瘤中展现出显著疗效。随着靶点筛选和连接子技术的持续创新,ADC 药物在前列腺癌治疗领域的开发也取得了重要进展。第一三共和默沙东的 Ifinatamab deruxtecan 是全球首个启动前列腺癌 III 期临床的 B7-H3 ADC,其在 mCRPC 患者中客观缓解率达 25%,中位无进展生存期 4.8 个月。此外,PSMA、STEAP1、TROP2、CD46 等靶点的 ADC 管线也显示出初步疗效。
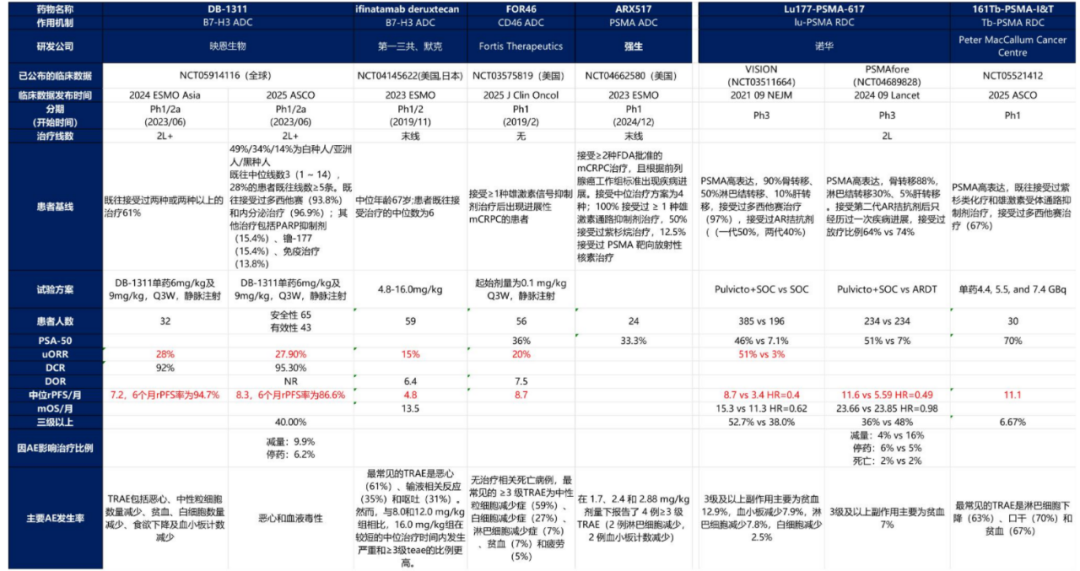
图:治疗前列腺癌的 ADC 疗法数据对比,来源:东吴证券
在免疫治疗领域,尽管单药效果有限,但免疫联合方案还是有望实现 1+1>2 的效果。目前 III 期试验探索 Pluvicto 联合 PD-1 抑制剂,早期数据显示 ORR 提升至 55%,中位 PFS 延长至 12 个月;PD-1 抑制剂联合奥拉帕利的方案在 HRR 突变患者中,疾病控制率达到 80%,证实了协同控制效果。
这些创新疗法的崛起,正在重新定义晚期前列腺癌的治疗格局。PARP 抑制剂、核素治疗等创新疗法,搭配早期 PSA 筛查,让部分患者甚至有望实现“ 功能性治愈”。从手术去势到精准靶向,历经八十多年探索,前列腺癌治疗终于穿越漫长黑暗,迎来破晓时分,迈向一个全新的黎明。
更多精彩内容,关注钛媒体微信号 (ID:taimeiti),或者下载钛媒体 App





















