文 | 氨基观察,作者 | 沙晓威
免疫治疗进入“ 后 PD-1 时代”,迭代与突破正成为主旋律。
当众多创新靶点尚在验证途中,BioNTech 正选择将目光重新投向 CTLA-4 这一老靶点身上。
作为全球首个问世的免疫检查点抑制剂,CTLA-4 抑制剂高开低走后沉寂许久。在最新研发日中,BioNTech 则将新一代 CTLA-4 单抗 Gotistobart 纳入优先免疫调节管线,沉寂多年的 CTLA-4 再度回归行业视野。
凭借分子设计的双重创新,Gotistobart 在早期临床中展现出增效减毒的潜力,提高了安全性窗口与持续疗效,为 PD-1 耐药患者带来突破性希望。
眼下,BioNTech 把 CTLA-4 重新推到幕前,意在抢夺下一代 IO 的基石。创新总是有着矛盾而迷人的两面性,不到最后一刻,永远不能对一款药物下结论。
那么,老靶点的新生,会成为下一代免疫治疗的破局关键吗?
/ 01 / 老靶点的新生
在免疫治疗的发展历程中,CTLA-4 的发现早于 PD-1,却走出了截然不同的发展轨迹。作为首个打开免疫治疗大门的靶点,CTLA-4 单抗以全身免疫激活的机制开辟了全新治疗路径,但也因固有缺陷长期处于 PD-1 的光环之下。
与 PD-1 单抗 20 余款产品上市盛况不同,截至目前,全球获批的 CTLA-4 单抗仅有两款,分别是百时美施贵宝的 Ipilimumab(Y 药) 和阿斯利康的 Tremelimumab。市场表现也与 PD-1 抑制剂相差悬殊:2024 年,K 药的全球销售额近 300 亿美元,而 Y 药的同期销售额仅为 25.3 亿美元,不足 K 药的十分之一,甚至一大部分的占比是基于与 PD-1 单抗 Nivolumab 联用的适应症。

安全性问题是制约 CTLA-4 抗体发展的核心瓶颈之一。早期 CTLA-4 抗体的作用机制直接:通过无差别抑制削弱 Tregs 的免疫抑制作用,进而激活全身免疫反应。缺点就是无法区分肿瘤与正常组织中的 Tregs,易引发严重的免疫相关不良反应 (IrAEs)。
疗效上的劣势则让 CTLA-4 彻底被 PD-1 掩盖。
2014 年,K 药、O 药相继上市,CTLA-4 抗体在黑色素瘤、非小细胞肺癌 (NSCLC) 等核心适应症中表现逊色。以黑色素瘤为例,Y 药治疗的客观缓解率 (ORR) 仅 10%-15%,而 K 药的 ORR 可达 30%-40%,部分亚型甚至能突破 50%。
即便是联合治疗场景,CTLA-4 抗体也多处于“ 辅助地位”。比如 Tremelimumab 目前获批的适应症均为与 O 药联合治疗。
尽管发展受限,CTLA-4 的研究从未停滞,而是朝着精准化方向转型。BioNTech 从 OncoC4 引进的新一代 CTLA-4 单抗 Gotistobart 正是这一转型思路的典型代表,其分子设计通过双重创新实现了对传统 CTLA-4 抗体的突破。
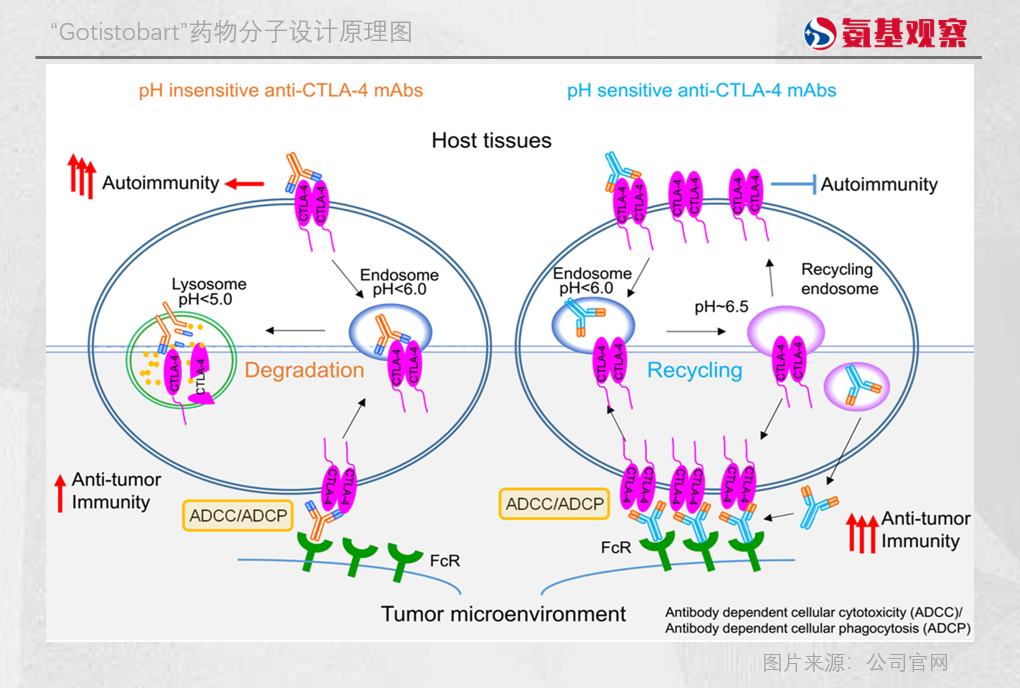
一方面,借助 pH 敏感型抗体技术,Gotistobart 与 CTLA-4 结合形成的复合物被细胞内吞后,会在溶酶体的酸性环境中发生解离,使 CTLA-4 蛋白能够重返细胞表面重新发挥作用,避免了传统抗体导致的 CTLA-4 内吞降解,大幅提升了药物的治疗窗口。
另一方面,通过 Fc 段的工程化改造,Gotistobart 能够更高效地招募免疫效应细胞,精准清除 TME 中的 Tregs,同时减少对正常组织的影响。
正如 OncoC4 所言,这种机制使 Gotistobart 具备了长期、重复给药的潜力,为持续控制肿瘤提供了可能。
早期临床数据初步验证了其潜力:在针对 ICI 耐受的 NSCLC 患者开展的 1/2 期临床试验中,Gotistobart 单药治疗的 ORR 达 29.6%,DCR 高达 70.4%,这一结果对 PD-1 耐药人群具有突破性意义。
基于此,今年 10 月,该药物获得 NMPA 授予的突破性疗法认定,用于治疗 PD-1 耐药的晚期 NSCLC 患者,成为首个在该适应症中获得突破性认定的新一代 CTLA-4 抗体。
/ 02 / BioNTech 的 IO 双支柱
将 Gotistobart 纳入优先免疫调节管线,是 BioNTech 构建下一代 IO 治疗体系的关键布局。
在其优先免疫调节剂研发管线中,PD-L1/VEGF 双抗 Pumitamig 与 CTLA-4 单抗 Gotistobart 构成两大核心支柱,分别代表了多靶点协同增效与老靶点升级改造的发展策略。
作为 BioNTech 重点布局的下一代 IO 基石,Pumitamig 的核心优势在于同时结合 PD-L1 与 VEGF 两个靶点,一方面阻断 PD-1/PD-L1 信号通路,激活效应 T 细胞的抗肿瘤功能,另一方面抑制 VEGF 介导的肿瘤血管生成,改善肿瘤微环境。
目前,BioNTech 已推动 Pumitamig20 项临床落地,除了小细胞癌、NSCLC 和三阴性乳腺癌的三期临床,更是加速推进泛癌种布局以及与化疗、ADC、新型免疫靶点药物 (如 PVRIG 抑制剂 BNT3213) 等不同且新颖的联合疗法研究。

相比之下,尽管是首次进入 BioNTech 的重点研发项目名单,但从即将推进的研究布局来看,Gotistobart 的定位绝非对现有 IO 药物的简单补位,而是要成为 BioNTech 下一代 IO 治疗的核心基石之一。
BioNTech 在研发日中明确提出,Gotistobart 的研发目标是“ 探索新的组合以确定潜在的未来治疗标准”。Gotistobart 的“ 魅力” 在于循环利用的机制以及针对 PD-1 耐药人群的潜力,这为其开展多样化的联合治疗研究提供了基础。
从研发日的报告上看,BioNTech 计划围绕 Gotistobart 启动了覆盖多个癌种、多种联合模式的研究:开展单药治疗针对二线及以上鳞癌 NSCLC 患者的 3 期临床试验,明确单药治疗潜力;开展联合 K 药治疗宫颈癌的 2 期研究,以明确 CTLA-4、PD-1 的协同效应潜力;还有联合核药 PLUVICTO 治疗转移性去势抵抗性前列腺癌的早期研究;以及开展覆盖多种实体瘤的早期临床研究,进一步挖掘潜在肿瘤适应症。
其中,与 PLUVICTO 联合治疗前列腺癌的研究极具看点。2025 年 ASCO 大会公布的 1 期研究初步结果显示,该联合方案耐受性良好,且临床前模型已证实,放射治疗能够选择性扩增并激活肿瘤微环境中的 Tregs,这恰好与 Gotistobart 的作用机制匹配
此外,Gotistobart 与 mRNA 疫苗 BNT116 的联合研究也已启动,借助 mRNA 疫苗引导 T 细胞向肿瘤抗原特异性分化的能力,结合 Gotistobart 清除免疫抑制细胞的作用,有望实现更持久的抗肿瘤免疫记忆。
尽管 Gotistobart 目前还处于早期适应症扩张和验证阶段,但是 BioNTech 的双支柱策略已经清晰:Pumitamig 通过多靶点协同作用提升免疫治疗疗效,覆盖广泛实体瘤治疗需求;Gotistobart 目前则聚焦 PD-1 耐药以及肿瘤晚期等难治人群,两者构成了肿瘤全周期的免疫治疗。
/ 03 / CTLA-4 值得期待
Gotistobart 的进展与 BioNTech 的战略布局只是 CTLA-4 赛道升温的一个缩影,全球药企正从分子设计优化、双抗研发、联合治疗等多个维度挖掘这一靶点的潜力。
在单抗领域,Agenus 公司的 Botensilimab 采用人源化 Fc 段增强设计,通过强化 ADCC 效应提升对肿瘤微环境中 Tregs 的清除效率,与 ipilimumab 相比,能同时激活先天与适应性免疫系统,尤甚至在冷肿瘤中表现潜力。其在与 Balstilimab(PD-1 抑制剂) 联合治疗微卫星稳定型转移性结直肠癌患者的 2 期临床中,实现了 42% 的两年生存率,平均 OS 为 20.9 个月,而对于已经接受过 4 线或更多治疗的患者,BOT/BAL 的联合治疗方案可以实现两年生存率 43%,ORR 为 19%。
国产药企在 CTLA-4 靶点的设计同样表现亮眼,比如和铂医药的 HBM4003。作为一款全人源重链抗 CTLA-4 抗体,HBM4003 仅有 76kDa,小分子的优势,能够更高效穿透肿瘤组织,提升肿瘤微环境中的药物浓度,同时,其 Fc 段经过突变改造,显著增强 ADCC 活性,可精准清除高表达 CTLA-4 的肿瘤浸润 Tregs。
不久前公布的 2 期临床数据显示,在既往接受过多种治疗的 MSS 转移性结直肠癌患者中,每 21 天接受 HBM4003 联合替雷利珠单抗治疗的 ORR 达 34.8%,DCR 60.9%,mPFS 为 4.2 个月,且 87.5% 的相关不良事件为 1、2 级,安全性表现优异。
双抗成为 CTLA-4 靶点的另一重要研发方向。康方生物的 AK104 是一款 CTLA-4/PD-1 双抗,同时阻断两个免疫检查点,实现协同激活免疫的效应。
尽管热度低于 PD-1/VEGF 双抗依沃西,但公司计划通过联合策略挖掘其价值,近期宣布 AK104 与依沃西联用治疗胰腺癌术后辅助治疗的 1 期临床已完成首例给药。
阿斯利康的 Volrustomig 同样是针对 PD-1/CTLA-4 的双抗,目前正在在 NSCLC 领域的研究正开展头对头 K 药的 3 期临床 eVOLVE-Lung02,进度与实力不容小觑。
联合治疗则持续拓展着 CTLA-4 的应用边界。BMS 的“Y 药+O 药” 组合已在黑色素瘤、NSCLC、肾癌等多个癌种中获得 FDA 批准,涉及十余项适应症;Tremelimumab 与 O 药的联合方案已获批用于 NSCLC 治疗,与 O 药+铂类化疗的三联方案则拓展至前列腺癌一线。
信达生物的 IBI310 则是国内研发进度领先的 CTLA-4 抗体,其与 PD-1 抑制剂信迪利单抗的联合方案在今年 2 月被 CDE 纳入优先审批,适应症为可切除的微卫星高度不稳定型或错配修复缺陷型结直肠癌患者的新辅助治疗。
此外,CTLA-4 抗体与 ADC、核药、小核酸等新型疗法的联合也是研究方向,BioNTech 探索的 Gotistobart 与核药 PLUVICTO 的联合,不仅是适应症的拓展也是机制的补充,为靶点价值的挖掘开辟了更多可能。
总之,CTLA-4 凭借独特的免疫调节机制与持续迭代的药物研发,有望摆脱 PD-1 的阴影,与多靶点药物、新型疗法形成协同,构建下一代 IO 治疗的基石。
尤其是当 PD-1 的耐药及不敏感问题成为免疫治疗的核心挑战之际,CTLA-4 则提供了另一条免疫调节途径。
尽管过程仍充满挫折和不确定性,但是创新药的发展,从来都是螺旋上升的。随着新技术、新机制的出现,以及更多临床数据的涌现,那些曾经被否定的药物,也有可能重新焕发新的光芒。
老靶点的新生,值得期待。
更多精彩内容,关注钛媒体微信号 (ID:taimeiti),或者下载钛媒体 App